
L’assunzione di liquidi viene controllata da due principali variabili fisiologiche: l’osmolarità tessutale e il volume del liquido intravascolare, ma anche dalla secchezza della lingua e dall’ipertermia
L’ipotalamo regola sia il bilancio idrico, attraverso azioni fisiologiche dirette, sia alcuni aspetti comportamentali relativi all’assunzione di liquidi.
L’assunzione di liquidi viene controllata da due principali variabili fisiologiche: l’osmolarità tessutale e il volume del liquido intravascolare, ma anche dalla secchezza della lingua e dall’ipertermia che viene rilevata, almeno in parte, dai neuroni termosensitivi dell’ipotalamo.
Nel corpo sono presenti quattro principali componenti liquidi, uno di liquido intracellulare e tre di liquido extracellulare.
Nel liquido intracellulare, ossia la componente fluida del citoplasma cellulare, sono compresi i due terzi del patrimonio idrico corporeo.
Il liquido extracellulare, che comprende il liquido intravascolare, il liquor cerebrospinale e il liquido interstiziale, rappresenta la parte rimanente. I diversi compartimenti liquidi sono separati tra loro da barriere semipermeabili. Le pareti dei capillari separano il liquido intravascolare dal liquido interstiziale, mentre le membrane cellulari separano il liquido interstiziale dal liquido intracellulare.
Il volume del liquido intracellulare è regolato attraverso il controllo della concentrazione dei soluti presenti nel liquido interstiziale che normalmente è isotonico rispetto al liquido intracellulare. La deplezione di acqua dal compartimento intracellulare attiva la cosiddetta sete osmometrica.
Il volume del plasma è regolato in modo tale da mantenere una buona funzione cardiaca. La deplezione di acqua dal compartimento intravascolare attiva la cosiddetta sete volumetrica.
La sete osmometrica è indotta da un aumento della concentrazione di soluti nel liquido interstiziale. L’ipertonicità del liquido interstiziale spinge l’acqua fuori dalle cellule, riducendo il volume cellulare e stimolando gli osmorecettori, neuroni la cui frequenza di scarica è influenzata dal livello di idratazione.
Gli osmorecettori cerebrali, che controllano la sete osmometrica, sono localizzati in una regione detta lamina terminale, situata appena rostralmente alla porzione ventrale del terzo ventricolo. La lamina terminale contiene due organi circumventricolari: l’OVLT (organum vasculosum della lamina terminale), e l’OSF (organo subfornicale). Essi sono posti sul lato ematico della barriera ematoencefalica, per cui le sostanze disciolte nel sangue diffondono facilmente nel liquido interstiziale all’interno di questo organo. Si ritiene che la maggior parte degli osmorecettori, responsabili della sete osmometrica, sia localizzata nell’OVLT. L’OSF contiene neuroni che rilevano la presenza di angiotensina nel sangue, attivando di conseguenza i circuiti neuronali che suscitano la sete.
Studi effettuati sui ratti hanno evidenziato che il nucleo preottico mediano, (un nucleo che è situato tra i due organi circumventricolari e avvolge la porzione frontale della commessura anteriore), è fortemente attivato dagli stimoli osmotici. Dalle lesioni di questo nucleo è emerso che può giocare un ruolo cruciale nella generazione della sete in risposta a segnali, sia osmotici che ormonali, che vi giungono dall’OSF e dall’OVLT. Il nucleo preottico mediano, che è ricco di recettori di tipo 1 per l’angiotensina, oltre a ricevere afferenze neuronali dai neuroni dell’OSF e OVLT può integrare questi segnali neuronali con altri provenienti da strutture romboencefaliche (come l’area postrema).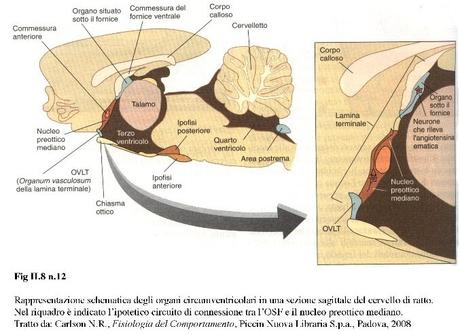
È stata dimostrata la presenza di un sistema renina-angiotensina cerebrale, con tutti i componenti della cascata metabolica. Si ritiene che l’angiotensina II circolante stimoli la sete agendo sugli organi circumventricolari (in particolare OSF) e che il sistema renina-angiotensina cerebrale e quello renale, sebbene distinti, siano funzionalmente accoppiati per mantenere l’omeostasi dei fluidi corporei.
La sete volumetrica insorge quando il volume intravascolare diminuisce, in quanto l’ipovolemia comporta oltre alla perdita di liquidi, anche una perdita di sodio. La rilevazione dell’ipovolemia e dell’iposodiemia viene effettuata da almeno due gruppi di recettori che svolgono questa doppia funzione: un gruppo nei reni, che controlla la secrezione di angiotensina, e un altro nel cuore e nei vasi sanguigni di grosso calibro (barorecettori atriali).
I recettori di volume a livello renale registrano le diminuzioni di apporto ematico e secernono renina, che catalizza la conversione di angiotensinogeno in angiotensina I, poi convertita in angiotensina II. L’angiotensina II promuove la ritenzione di sodio e di acqua, aumenta la pressione arteriosa promuovendo la contrazione della muscolatura liscia arteriolare, dà impulso all’assunzione di liquidi e determina fame di sale.
Il secondo gruppo di recettori di volume è localizzato a livello degli atri cardiaci. La distensione della regione dell’atrio destro, della vena cava o della vena polmonare, all’entrata dell’atrio sinistro, può inibire la sete indotta sperimentalmente. Gli impulsi afferenti, provenienti dai barorecettori atriali e cardiopolmonari, arrivano al cervello tramite il IX e il X nervo cranico e terminano a livello del nucleo del tratto solitario (NTS), che invia assoni efferenti a molte regioni cerebrali. In particolare, dalle regioni del NTS, ma anche dall’area postrema (AP) partono assoni che proiettano prima al nucleo laterale parabrachiale (LPBN) e da qui al nucleo preottico mediano.
I meccanismi della sete vengono influenzati anche da diversi ormoni (peptidi e steroidi). Alcuni peptidi come l’oressina e la relaxina stimolano la sete, altri come il peptide natriuretico atriale e il glucagon-like-peptide-1 la inibiscono.
La relaxina è secreta dal corpo luteo dell’ovaio durante la gravidanza. Si è visto che, se somministrata centralmente o per via sistemica nei ratti, influenza l’omeostasi dei liquidi sia stimolando la secrezione di vasopressina, sia l’assunzione di acqua. I recettori della relaxina sono presenti in alte concentrazioni sia nell’OSF, sia nell’OVLT, ma si ritiene che l’OSF sia il sito principale responsabile dell’azione della relaxina somministrata per via endovenosa. Durante la gravidanza i livelli osmolari plasmatici cadono e ciò dovrebbe esercitare un’influenza inibitoria sui meccanismi della sete. Tuttavia, l’assunzione di acqua è mantenuta o anche aumentata nonostante l’ipotonicità plasmatica e la relaxina, secreta durante la gravidanza, potrebbe essere uno dei fattori che promuovono l’assunzione di liquidi.
Il peptide natriuretico atriale ANP (Atrial Natriuretic Peptide) è rilasciato dai miociti degli atri cardiaci in risposta allo stiramento atriale e diversi altri segnali. I fattori che attivano la secrezione di ANP sono i seguenti:
- Distensione atriale (attivata da un aumento dei fluidi extracellulari e del volume ematico, dalla fibrillazione atriale, da immersioni subacquee e dall’attività fisica intensa).
- Stimolazione simpatica dei β-recettori.
- Ipernatremia, sebbene la concentrazione di Na+ non stimoli direttamente la secrezione di ANP.
- Angiotensina II.
- Endotelina, un potente vasocostrittore.
L’ANP si lega a specifici recettori (ANP receptors) e contrasta l’incremento di pressione arteriosa e l’incremento di volume provocati dal sistema renina-angiotensina. In generale, l’ANP ha una potente azione inibitoria sull’assunzione di liquidi e inibisce la secrezione di vasopressina. Sembra agire inibendo la sete stimolata dall’angiotensina II agendo direttamente sull’OSF.
I neuroni ipotalamici che liberano vasopressina (ADH) sono spontaneamente attivi, assicurano la presenza nel sangue di concentrazioni basali di ormone, ricevono input sinaptici dagli osmorecettori della lamina terminale e sono stimolati da:
- Variazione della pressione osmotica del plasma e variazione della concentrazione ematica di sodio. Questi stimoli agiscono direttamente sugli osmorecettori ipotalamici. Quando l’organismo è disidratato o la concentrazione di Na+ è elevata, i neuroni ipotalamici che liberano ADH scaricano a frequenza più elevata e presentano un’attività a raffica.
- Variazione di volume dei liquidi extracellulari. La riduzione del volume ematico aumenta la sintesi di ADH. Le variazioni di volume del liquido intravasale vengono rilevate da recettori di volume, localizzati nell’atrio destro e nelle pareti delle grandi vene, e le afferenze vengono inviate all’ipotalamo. Quando le variazioni di volume sono molto ampie intervengono anche i barocettori dell’arco dell’aorta e del seno carotideo. La riduzione del volume ematico può determinare anche un aumento della secrezione di renina da parte del rene e quindi la sintesi di angiotensina II.
- Angiotensina II. L’angiotensina II promuove l’assunzione di liquidi e riduce le perdite idriche mediante tre azioni fisiologiche: vasocostrizione; aumento della liberazione di aldosterone; aumento della liberazione di ADH. L’angiotensina II agisce stimolando i neuroni dell’OFS che inviano proiezioni al nucleo preottico mediano.
Le diverse informazioni che giungono all’ipotalamo vengono integrate e convogliate a diverse regioni cerebrali implicate nel comportamento che porta alla ricerca dell’acqua e alla sua assunzione.
Per ulteriori approfondimenti su questo argomento si rinvia al testo Multidisciplinarietà in Medicina.
Hai un account google? clicca su:

